Команда ученых под руководством Медицинской школы им. Гроссмана при Нью-Йоркском университете описала механизм, который помогает раковым клеткам поджелудочной железы избежать «голода» в плотных опухолях.
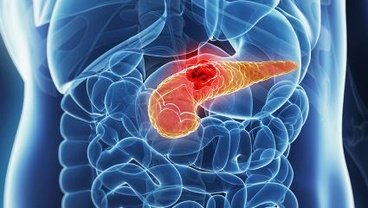 Ученые объяснили, как изменения в гене RAS, которые способствуют аномальному росту опухоли, характерному для 90% пациентов с раком поджелудочной железы, ускоряют процесс (макропиноцитоз), который обеспечивает этот рост необходимыми строительными блоками.
Ученые объяснили, как изменения в гене RAS, которые способствуют аномальному росту опухоли, характерному для 90% пациентов с раком поджелудочной железы, ускоряют процесс (макропиноцитоз), который обеспечивает этот рост необходимыми строительными блоками.
Макропиноцитоз вызывает поглощение белков и жиров, которые могут быть разделены на аминокислоты и метаболиты, используемые для создания новых белков, цепей ДНК и клеточных мембран. Раковые клетки не могут размножаться без этих ресурсов.
Опубликованное в журнале «Nature» исследование определяет ключевые молекулярные этапы, которые вызываются раковыми клетками для усиления микропиноцитоза.
«Мы нашли механизм, связанный со снабжением рака питательными веществами, который, как мы полагаем, может быть использован для того, чтобы лишить RAS-мутантные опухолевые клетки ключевого механизма выживания» - сообщили ученые.
В частности, исследовательская группа обнаружила, что мутации RAS дополнительно активируют белок SLC4A7, который позволяет белку, называемому бикарбонат-зависимой растворимой аденилатциклазой, активировать фермент протеинкиназу А. Это, в свою очередь, способствует изменению местоположения белка v-ATPase.
Ученые сообщили, что благодаря смещению vATPase из глубины клеток к области рядом с внешними мембранами, происходит прикрепление RAC1 к клеточным мембранам. Наращивание v-ATPase возле внешних мембран и связанное с этим расположение Rac1 позволяют мембранам временно выпирать и формировать поглощающие питательные вещества карманы (везикулы) во время макропиноцитоза.
В исследованиях на клеточных культурах обработка мутантных клеток RAS ингибитором семейства SLC4 S0859 привела к значительному уменьшению RAS-зависимой локализации vATPase на наружных мембранах, а также к ингибированию микропиноцитоза.
Кроме того, анализ молекулярных данных из ткани аденокарциномы протоков поджелудочной железы человека показал, что ген SLC4A7 экспрессируется в четыре раза сильнее в опухолях, чем в нормальной ткани поджелудочной железы.
Ученые также продемонстрировали, что заглушка гена SLC4A7 в клетках рака поджелудочной железы замедлило или уменьшило опухоли у мышей. Через 14 дней у 62% опухолей с заглушенным SLC4A7 уменьшился рост, по сравнению с опухолями, в которых ген SLC4A7 был активным, а 31% опухолей уменьшились в объеме.
SLC4A7 и v-ATPase являются многообещающими лекарств мишенями, поскольку они связаны с ростом рака и действуют вблизи поверхности раковых клеток, что облегчает доставку терапевтических агентов.
«Сейчас мы ищем лекарственные средства, которые могут ингибировать действие SLC4A7 или v-ATPase, в качестве возможных методов лечения, блокирующих макропиноцитоз» - сообщили ученые.
Источник: https://www.sciencedaily.com/releases/2019/12/191211144933.htm






Комментарии
Пока комментариев нет
Новый комментарий